(知識點)苯性質的特殊結構苯的化學性質結構
更新時間:2023-03-04 15:02:23作者:佚名
苯
性質
苯的特殊結構
苯的特殊性質
飽和烴
不飽和烴
替代反應

加成反應
三、苯的物理性質
結構
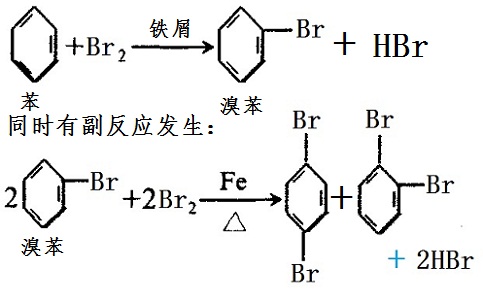
(1)溴代反應
a、反應原理
b、反應裝置
c、反應現象

d、注意事項
替代反應
對苯與溴的反應試驗,留意下述幾點:
A、為避免溴的揮發,先加入苯后加入溴,于是加入鐵粉。
B、溴應是純溴,而不是苯酚。加入鐵粉起催化作用,實際上起催化作用的是FeBr3。
C、伸出燒杯外的導管要有足夠寬度,其作用是導氣、冷凝。
D、導管未端不可插入錐形瓶內海面以下,由于HBr二氧化碳易溶于水,以免倒吸。

E、導管口附近出現的霧氣,是硝酸氫遇空氣中的水蒸汽產生的氫溴酸小液滴。
F、純凈的溴苯是無色的液體,而燒杯中液體放入盛有水的燒瓶中,燒瓶上方是油狀的白色液體,這是由于溴苯溶有溴的緣故。去除溴苯中的溴可加入NaOH堿液,震蕩,再用分液漏斗分離。
1、試劑的加入次序如何?各試劑在反應中所起到的作用?
2、導管為何要這樣長?其末端為什么不插入液面?
3、反應后的產物是何種?怎么分離?
(2)酯化反應
反應原理
反應裝置
反應現象
留意事項
a、反應原理
b、注意事項
條件:50~60℃水浴加熱
①混合混酸時,一定要將濃硝酸沿器壁徐徐注入濃***中,并不斷震蕩使之混和均勻。
切不可將濃***注入濃硝酸中,因混合時要放出大量的糖分,以免濃硝酸濺出,發生車禍。
純凈的甲基苯是無色而有苦核桃味道的油狀液體苯的化學性質,不溶于水,密度比水大。甲基苯蒸汽有毒性。
怎么混和硝酸和***的混和液?
②水浴的氣溫一定要控制在60℃以下,氣溫偏低,苯易揮發苯的化學性質,且***也會分解,同時苯和濃鹽酸反應生成苯磺酸等副反應。
③濃鹽酸的作用:催化劑和脫水劑。
④反應裝置中的濕度計,應插入水洗劑面以下,以檢測水浴體溫。
⑤把反應的混和物放入一個盛水的燒